

弁膜疾患の非薬物治療に関するガイドライン(2012年改訂版)
Guidelines for Surgical and Interventional Treatment of Valvular Haert Disease( JCS 2012)
報告者年平均追跡期間
(年)
植込み弁数推定人工
弁構造的
劣化期間
(年)
年齢
人工弁構造的劣化非発生率
コメント
AVR MVR AVR MVR
Yu, et al 2003 8.9 161 523 12.2 20 43.1 Carpentier-Edwards
(JTCVS2003) 20~40 64.9 standardブタ生体
40~60 65.5 弁
60 74.1
Jamieson, et al 2006 7.9 1,825 15 40 48.4 Carpentier-Edwards
(ACTA2006) 41~50 63.1 supraannular ブタ生体
51~60 75.4 弁
61~70 93
70 98.2
Borger, et al 2006 7.4 1,010 559 20 <65 39 27 Hancock Ⅱブタ生体弁
(JHVD2006) 65 73 59
Jamieson, et al 2011 7.5 797 232 12 <65 79.4 94.3 Mosaic ブタ生体弁
(JTCVS2011)
65 95.9 95.1
McClure, et al 2010 8.3 1,000 15 <65 34.7 Carpentier-Edwards
(Ann Thorac Surg2010) 65~75 89.4 牛心のう膜弁
75 99.5
Ayegnon, et al 2011 8.9 401 23 <60 8.6 Carpentier-Edwards
(ACTA) 60 20 牛心のう膜弁
ISTHMUS investigators 2011 7.4 1,591 18 <60 54.4 Mitroflow
(EJCTS2010) 60~70 62
70 78
(年)
植込み弁数推定人工
弁構造的
劣化期間
(年)
年齢
人工弁構造的劣化非発生率
コメント
AVR MVR AVR MVR
Yu, et al 2003 8.9 161 523 12.2 20 43.1 Carpentier-Edwards
(JTCVS2003) 20~40 64.9 standardブタ生体
40~60 65.5 弁
60 74.1
Jamieson, et al 2006 7.9 1,825 15 40 48.4 Carpentier-Edwards
(ACTA2006) 41~50 63.1 supraannular ブタ生体
51~60 75.4 弁
61~70 93
70 98.2
Borger, et al 2006 7.4 1,010 559 20 <65 39 27 Hancock Ⅱブタ生体弁
(JHVD2006) 65 73 59
Jamieson, et al 2011 7.5 797 232 12 <65 79.4 94.3 Mosaic ブタ生体弁
(JTCVS2011)
65 95.9 95.1
McClure, et al 2010 8.3 1,000 15 <65 34.7 Carpentier-Edwards
(Ann Thorac Surg2010) 65~75 89.4 牛心のう膜弁
75 99.5
Ayegnon, et al 2011 8.9 401 23 <60 8.6 Carpentier-Edwards
(ACTA) 60 20 牛心のう膜弁
ISTHMUS investigators 2011 7.4 1,591 18 <60 54.4 Mitroflow
(EJCTS2010) 60~70 62
70 78
クラスⅠ
1 易出血性疾患の合併などによりワーファリン投与が
不可能あるいはそれを拒否する患者
2 AVRを必要とする65歳以上の患者で血栓塞栓の危
険因子を持たない場合
クラスⅡa
1 ワーファリン投与のコンプライアンスに問題がある
と思われる患者
2 妊娠を希望する若い女性
3 活動性の感染性心内膜炎でAVRを必要とする患者に
対する同種弁によるAVR
4 TVRを必要とする患者
クラスⅡb
1 MVRを必要とする70歳以上の患者で血栓塞栓の危
険因子を持たない場合
2 血栓が形成された機械弁に対する再弁置換術
3 成長が期待される患者における自己肺動脈弁による
AVR
4 65歳未満であっても抗凝固療法のリスクと将来再
手術が必要となるリスクについて詳細に話し合った
結果,生体弁を選択した洞調律患者の場合
1 易出血性疾患の合併などによりワーファリン投与が
不可能あるいはそれを拒否する患者
2 AVRを必要とする65歳以上の患者で血栓塞栓の危
険因子を持たない場合
クラスⅡa
1 ワーファリン投与のコンプライアンスに問題がある
と思われる患者
2 妊娠を希望する若い女性
3 活動性の感染性心内膜炎でAVRを必要とする患者に
対する同種弁によるAVR
4 TVRを必要とする患者
クラスⅡb
1 MVRを必要とする70歳以上の患者で血栓塞栓の危
険因子を持たない場合
2 血栓が形成された機械弁に対する再弁置換術
3 成長が期待される患者における自己肺動脈弁による
AVR
4 65歳未満であっても抗凝固療法のリスクと将来再
手術が必要となるリスクについて詳細に話し合った
結果,生体弁を選択した洞調律患者の場合

2 生体弁の選択
(表53)
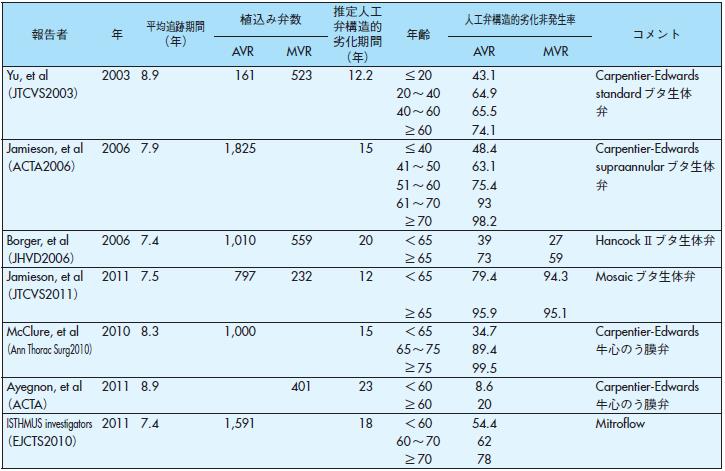
生体弁の主な長所は,前述のごとく弁の種類を問わず血栓塞栓症の発生が低く,抗凝固療法を必要としない,または軽減できるため,抗凝固療法に伴う出血の合併が低率であることである.生体弁の主な短所は構造的劣化率が比較的高く,再手術の必要性が高いことである(表54).生体弁の構造的劣化率は年齢や弁位に影響されるといわれており511)-513),523),526),527),530),543)-546),年長者や大動脈弁位および三尖弁位での劣化率は低率である.大動脈弁位における65歳以上の患者513),523),527),543),544)や,僧帽弁位における70歳以上の患者512),530),543),546)では生体弁の構造的劣化率が低いことより,患者が血栓塞栓の危険因子を持たない場合は生体弁のよい適応をもつと考えられている.(なお2006年に改訂されたACC/AHAの新ガイドライン1)では,僧帽弁位での生体弁選択の年齢基準を前回の70歳以上から今回65歳以上に引き下げているが,特にその理由は明記されておらず,またこれを支持する新しいdataが発表されたわけでもないため,本ガイドラインでは従来の方針を維持することとする.)
これより若い患者に対する生体弁の使用に関しては,抗凝固療法のリスクと将来再弁置換術が必要となるリスクについて患者と詳細に話し合った後に,術後の生活様式を考え生体弁を希望するのであれば,必ずしも禁忌にはならないと考えられる(表53).
三尖弁位における生体弁の構造的劣化率が低いことも知られている547)-549)が,適応に関しての明らかな証拠を得るまでには至っていない.
出血のリスクが高い合併症を有するなどの理由で抗凝固療法が不可能な場合や,患者が抗凝固療法を拒否する場合には生体弁の適応となる.また,抗凝固療法のコンプライアンスに問題があると考えられる患者にも生体弁の適応が考慮される.
弁置換術後に妊娠を考えている女性患者における人工弁選択には未だ議論のあるところであるが,抗凝固療法としてのワーファリンの投与は患者や胎児へのリスクとなるため550),551),妊娠分娩に関しては生体弁の方が機械弁に比し安全と一般的には考えられている552)-554).妊娠分娩が異種生体弁の構造的劣化に及ぼす影響については未だ明らかにされていない552)-554)が,患者年齢が若いことより前述のように将来再手術が避けられないことについて患者の同意を得る必要がある.異種生体弁に比し,自己弁や同種弁が有利と考えられている555)が,明らかな証拠はない.また,機械弁術後の妊娠,分娩時の抗凝固療法については,妊娠第1期は,ワーファリンによる催奇形性が問題になることからヘパリンないし低分子ヘパリンを投与,妊娠第2 期では,ワーファリンを投与し,妊娠第3期には,再び,ヘパリンに置換し,分娩に備えることが一般的である556)-558).
高カルシウム血症患者および小児患者等に生体弁を植込んだ場合には生体弁の構造的劣化率が高くなるため,通常生体弁は適応とならない.ただし,自己弁では成長の可能性があると考えられており,大動脈弁置換に限り自己弁による置換術(Ross 手術)は小児,若年者にもよい適応と考えられている.また,透析患者では生体弁を植込んだ場合には構造的劣化率が高いため,以前には生体弁は適応外とする報告もあったが,透析患者では元々長期予後が不良であることや抗凝固療法による出血性の合併症を考えると,人工弁の種類は予後に影響を与えないと報告434),440),449),559),560)されており,最近の傾向として,人工弁を選択する際に,透析の有無を考慮に入れる必要がないと考えられている.(2006年に改訂されたACC/AHAの新ガイドライン1)でも,透析患者での機械弁選択の項目が削除されている.)
再弁置換手術を施行する場合,再手術の理由が生体弁の機能不全であれば機械弁を,機械弁の血栓弁であれば生体弁を考慮するのが一般的である.また,十分な抗凝固療法下においても頻回に血栓塞栓症を合併する症例においても生体弁による再手術が考慮される.
いずれにしても生体弁選択にあたっては,構造的劣化による再手術の可能性と生体弁の有用性を患者に説明し,患者の意向を十分に考慮にいれながら決定しなければならない.
これより若い患者に対する生体弁の使用に関しては,抗凝固療法のリスクと将来再弁置換術が必要となるリスクについて患者と詳細に話し合った後に,術後の生活様式を考え生体弁を希望するのであれば,必ずしも禁忌にはならないと考えられる(表53).
三尖弁位における生体弁の構造的劣化率が低いことも知られている547)-549)が,適応に関しての明らかな証拠を得るまでには至っていない.
出血のリスクが高い合併症を有するなどの理由で抗凝固療法が不可能な場合や,患者が抗凝固療法を拒否する場合には生体弁の適応となる.また,抗凝固療法のコンプライアンスに問題があると考えられる患者にも生体弁の適応が考慮される.
弁置換術後に妊娠を考えている女性患者における人工弁選択には未だ議論のあるところであるが,抗凝固療法としてのワーファリンの投与は患者や胎児へのリスクとなるため550),551),妊娠分娩に関しては生体弁の方が機械弁に比し安全と一般的には考えられている552)-554).妊娠分娩が異種生体弁の構造的劣化に及ぼす影響については未だ明らかにされていない552)-554)が,患者年齢が若いことより前述のように将来再手術が避けられないことについて患者の同意を得る必要がある.異種生体弁に比し,自己弁や同種弁が有利と考えられている555)が,明らかな証拠はない.また,機械弁術後の妊娠,分娩時の抗凝固療法については,妊娠第1期は,ワーファリンによる催奇形性が問題になることからヘパリンないし低分子ヘパリンを投与,妊娠第2 期では,ワーファリンを投与し,妊娠第3期には,再び,ヘパリンに置換し,分娩に備えることが一般的である556)-558).
高カルシウム血症患者および小児患者等に生体弁を植込んだ場合には生体弁の構造的劣化率が高くなるため,通常生体弁は適応とならない.ただし,自己弁では成長の可能性があると考えられており,大動脈弁置換に限り自己弁による置換術(Ross 手術)は小児,若年者にもよい適応と考えられている.また,透析患者では生体弁を植込んだ場合には構造的劣化率が高いため,以前には生体弁は適応外とする報告もあったが,透析患者では元々長期予後が不良であることや抗凝固療法による出血性の合併症を考えると,人工弁の種類は予後に影響を与えないと報告434),440),449),559),560)されており,最近の傾向として,人工弁を選択する際に,透析の有無を考慮に入れる必要がないと考えられている.(2006年に改訂されたACC/AHAの新ガイドライン1)でも,透析患者での機械弁選択の項目が削除されている.)
再弁置換手術を施行する場合,再手術の理由が生体弁の機能不全であれば機械弁を,機械弁の血栓弁であれば生体弁を考慮するのが一般的である.また,十分な抗凝固療法下においても頻回に血栓塞栓症を合併する症例においても生体弁による再手術が考慮される.
いずれにしても生体弁選択にあたっては,構造的劣化による再手術の可能性と生体弁の有用性を患者に説明し,患者の意向を十分に考慮にいれながら決定しなければならない.
表53 生体弁による弁置換術の適応に関する推奨
表54 生体弁の構造的劣化
Ⅴ その他 >
6 生体弁の適応と選択 >
2 生体弁の選択(表53)